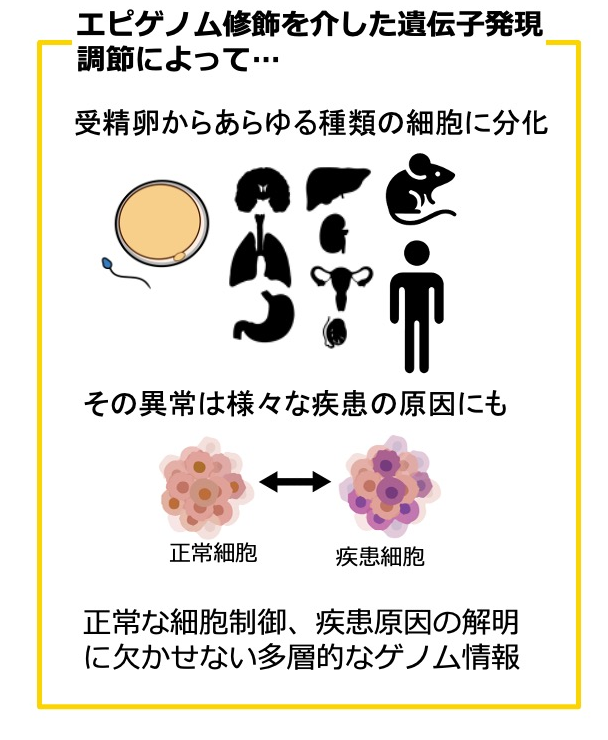
生物個体を形成するさまざまな種類の細胞は、いずれも同じDNA情報を持ち、その同じ設計図から、多様な種類の多様な量のRNAがコピーされ、 これを基に必要なタンパク質が作られ、それぞれの細胞の性質が決まります。その各遺伝子から産出されるRNAのコピー量は通常、遺伝子発現 レベルとしてプロファイリングされ、細胞種特異的な情報として、その多彩な細胞・組織の表現型や疾患と関連付けられます。
そして、「同じ設計図」のDNAから、細胞種特異的にその遺伝子発現レベルをコントロールする仕組みとして、エピゲノム制御 機構があります。DNAはヒストンという小さなタンパク質に巻きついて、クロマチンという構造体としてコンパクトに核内に収納されています。その ヒストンにメチル化、アセチル化、ユビキチン化といった修飾が施され、またDNA自体にもDNAメチル化修飾などが付加され、クロマチン構造が緩んだり閉じたりして、各ゲノム領域の転写機構が促進または抑制されます。こうした遺伝子発現制御につながるクロマチンへの化学修飾を「エピゲノム修飾」と呼び、細胞種特異的および疾患特異的な情報として、DNAに可塑的に維持され、その多様な表現型を可能にしています。
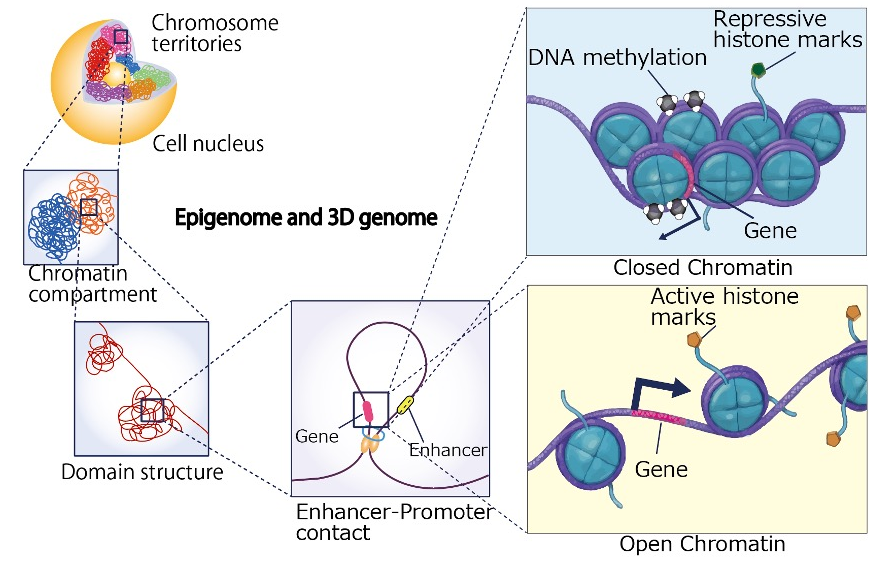
上述のようにクロマチン構造として核内に収納されているDNAは、ヒトやマウスで30億塩基対にも及び、1つの細胞の中にあるDNAをつなげると、約2メートルにもなると言われています。そして、それは決して雑に核内に収納されているのではなく、ある程度整然とした3次元的な構造(3Dゲノム 構造)を持って折り畳まれています。
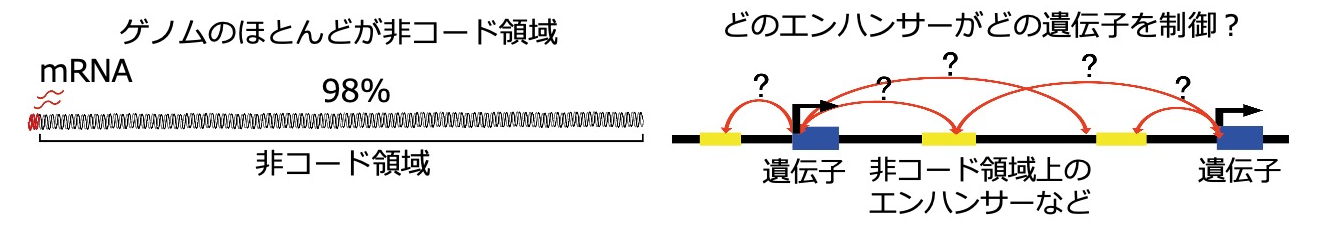
一方でそのDNAのほとんどが、タンパク質をコードする遺伝子"以外"の非コード領域 であるとされています。重要なことに、その非コード領域にもさまざまなエピゲノム修飾が施され、エンハンサーなど遺伝子の転写調節に関わる機能的なゲノム領域が数多く存在しています。ただし、その非コード領域上に種々のエピゲノム修飾を同定し、活性型エンハンサー領域を予測できたとしても、それがどの遺伝子の制御に関わっているのか不明なままです。そこで、エンハンサー領域とプロモーター領域を結ぶ DNAループ構造をはじめとする 3Dゲノム情報が重要なヒントを我々に与えてくれます。
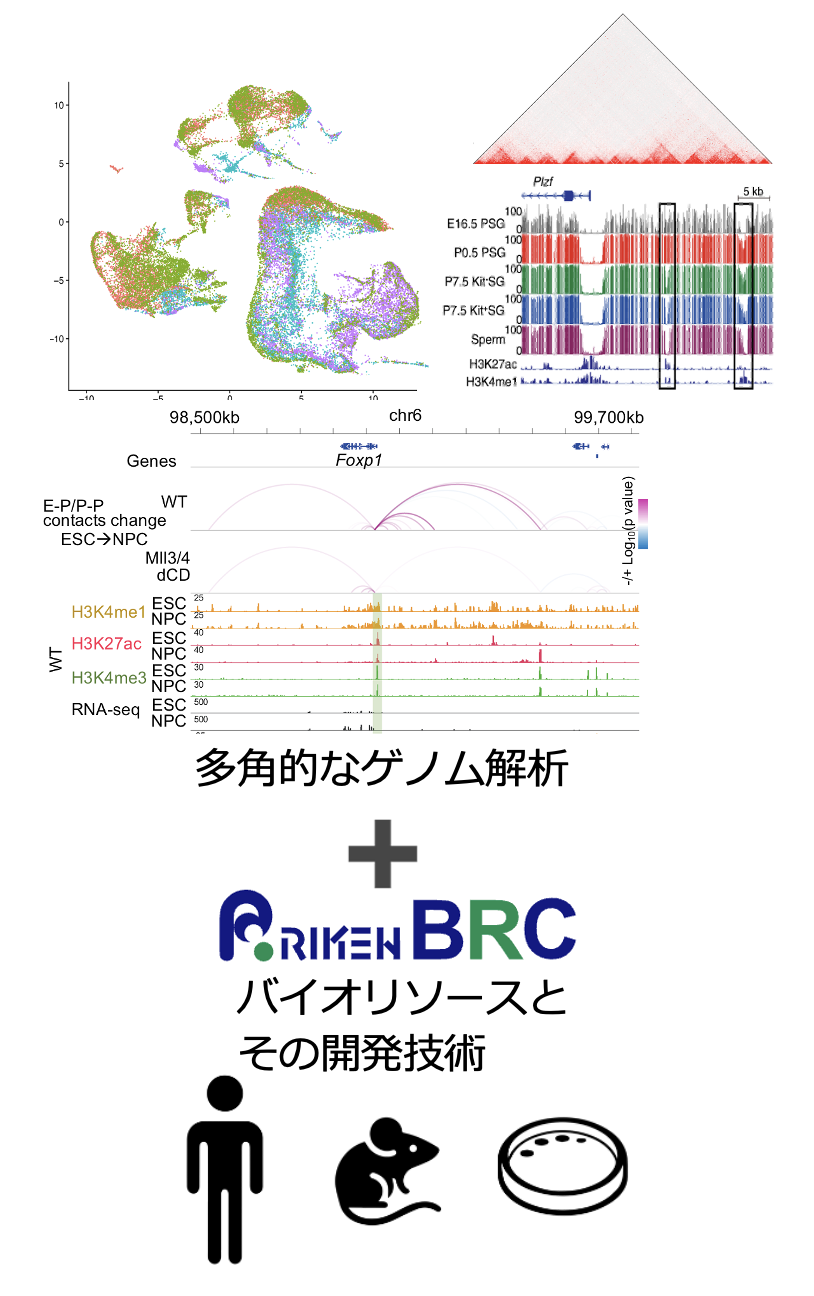
これまで我々は、こうしたエピゲノム制御機構や転写制御装置としての3Dゲノム構造の研究を、さまざまな最新の解析手法を用い、マウス生殖細胞やES細胞を舞台に行って参りました(業績)。
理研BRCでも、遺伝子発現解析や、エピゲノム・3Dゲノム解析のバルクおよびシングルセル解析の最新技術を導入および独自開発を行い、AI技術とそうした解析技術の融合で、BRCが保有する豊富なモデル動物やiPS細胞株をフルに活用し、生殖・発生や疾患特異的な遺伝子発現制御機構の探求を進めます。
遺伝子発現情報、エピゲノムおよび3Dゲノム情報を得る最新のバルクおよびシングルセル解析基盤の確立と新たな解析技術の開発
それらの解析技術を用いた、遺伝子発現制御メカニズムの解明および生殖・発生や疾患特異性に焦点を当てた研究
新たに得られるエピゲノムデータと蓄積データを活用した、ゲノム制御および表現型のAI予測モデルの構築
多彩なバイオリソースの表現型に対応する多角的ゲノムデータの取得とデータベース構築